Contenido
Los isótopos son átomos del mismo elemento que tienen diferentes números de neutrones en sus núcleos; Cuando se introducen en el cuerpo humano, se pueden detectar por radiación u otros medios. Los isótopos, utilizados junto con equipos sofisticados, brindan a los profesionales médicos una "ventana" poderosa en el cuerpo, permitiéndoles diagnosticar enfermedades, estudiar procesos biológicos e investigar el movimiento y el metabolismo de las drogas en personas vivas.
Isótopos estables e inestables
Los isótopos pueden ser estables o inestables; los inestables emiten radiación y los estables no. Por ejemplo, el átomo estable de carbono-12 constituye el 98.9 por ciento de todo el carbono en la Tierra; Debido a que el isótopo de carbono 14 más raro es radiactivo y cambia con el tiempo, los científicos lo usan para determinar la edad de los especímenes y materiales biológicos a veces antiguos. Químicamente, los isótopos estables e inestables actúan de la misma manera, lo que permite a los médicos sustituir los átomos radiactivos por los estables en los medicamentos utilizados para rastrear las actividades biológicas. Los isótopos estables, fácilmente identificables con un dispositivo llamado espectrómetro de masas, ayudan a los investigadores a determinar las condiciones en la sangre y los tejidos cuando la radioactividad no es deseable.
Investigación nutricional
Los isótopos estables ayudan a los científicos de nutrición a controlar el movimiento de minerales a través del cuerpo. Por ejemplo, de los cuatro isótopos estables para el hierro, el hierro-56 representa naturalmente alrededor del 92 por ciento, y el más raro es el hierro-58 con un 0,3 por ciento. Un científico administra a un sujeto de prueba dosis de hierro-58 y monitorea las cantidades de diferentes isótopos de hierro en sangre y otras muestras biológicas. Como el hierro 58 es más pesado que el hierro 56, un espectrómetro de masas los distingue fácilmente. Las primeras muestras mostrarán más hierro-56, pero con el tiempo, el hierro-58 se encontrará en cantidades significativas en diversos tejidos y sustancias, lo que permitirá al científico medir con precisión cómo el cuerpo del sujeto procesa el hierro.
Escaneos PET
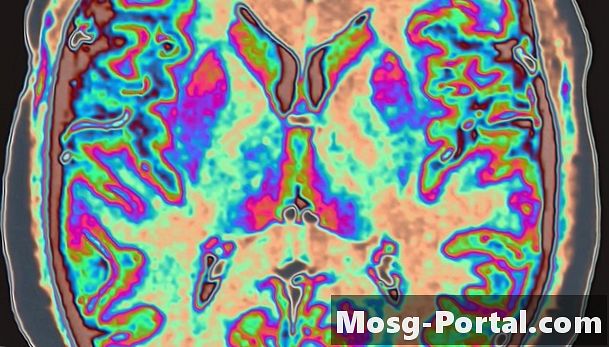
La tomografía por emisión de positrones produce imágenes tridimensionales de órganos y tejidos mediante el uso de isótopos radiactivos. Los isótopos, como el flúor-18, emiten radiación gamma, una forma de energía que pasa a través del cuerpo hacia un detector. Cuando se combina con azúcar y se administra a un paciente, el flúor migra a los tejidos que metabolizan activamente el azúcar, como las áreas del cerebro de una persona que trabaja en problemas matemáticos. Los escaneos PET muestran estas partes del cuerpo con detalles claros. Al observar los diferentes niveles de metabolismo, un médico puede identificar signos reveladores de anormalidades como tumores y demencia.
Escaneos MPI
Una exploración de imágenes de perfusión miocárdica utiliza isótopos radioactivos para producir imágenes en un método similar a una exploración PET, pero para monitorear el corazón en tiempo real. Según el Hospital de la Universidad de Stanford, la técnica emplea isótopos como el tecnecio 99 o el talio 201. Estos isótopos se inyectan en una vena y llegan al corazón. Una cámara especializada capta los rayos gamma emitidos y produce una imagen del corazón que late en condiciones de reposo y estrés, lo que permite al médico evaluar la salud del órgano.